22. Опыты Резерфорда по рассеянию 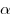 -частиц. Ядерная модель атома. Квантовые постулаты Бора -частиц. Ядерная модель атома. Квантовые постулаты Бора
1. Опыты Резерфорда. 2. Ядерная модель атома. 3. Постулаты Бора.. 4. Распространенные ошибки.
Слово «атом» в переводе с греческого означает «неделимый». Под атомом долгое время, вплоть до начала XX в., подразумевали мельчайшие неделимые частицы вещества. К началу XX в. в науке накопилось много фактов, говоривших о сложном строении атомов.
Большие успехи в исследовании строения атомов были достигнуты в опытах английского ученого Эрнеста Резерфорда по рассеянию 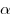 -частиц при прохождении через тонкие слои вещества. В этих опытах узкий пучок -частиц при прохождении через тонкие слои вещества. В этих опытах узкий пучок 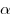 -частиц, испускаемых радиоактивным веществом, направлялся на тонкую золотую фольгу. За фольгой помещался экран, способный светиться под ударами быстрых частиц. Было обнаружено, что оолынинство -частиц, испускаемых радиоактивным веществом, направлялся на тонкую золотую фольгу. За фольгой помещался экран, способный светиться под ударами быстрых частиц. Было обнаружено, что оолынинство 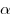 -частиц отклоняется от прямолинейного распространения после прохождения фольги, т. е. рассеивается, а некоторые -частиц отклоняется от прямолинейного распространения после прохождения фольги, т. е. рассеивается, а некоторые 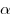 -частицы вообще отбрасываются назад. Рассеяние -частицы вообще отбрасываются назад. Рассеяние 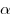 -частиц Резерфорд объяснил тем, что положительный заряд не распределен равномерно в шаре радиусом 10-10 м, как предполагали ранее, а сосредоточен в центральной части атома — атомном ядре. При прохождении около ядра -частиц Резерфорд объяснил тем, что положительный заряд не распределен равномерно в шаре радиусом 10-10 м, как предполагали ранее, а сосредоточен в центральной части атома — атомном ядре. При прохождении около ядра 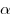 -частица, имеющая положительный заряд, отталкивается от него, а при попадании в ядро — отбрасывается в противоположном направлении. Так ведут себя частицы, имеющие одинаковый заряд, следовательно, существует центральная положительно зараженная часть атома, в которой сосредоточена значительная масса атома. Расчеты показали, что для объяснения опытов нужно принять радиус атомного ядра равным примерно 10-15 м. -частица, имеющая положительный заряд, отталкивается от него, а при попадании в ядро — отбрасывается в противоположном направлении. Так ведут себя частицы, имеющие одинаковый заряд, следовательно, существует центральная положительно зараженная часть атома, в которой сосредоточена значительная масса атома. Расчеты показали, что для объяснения опытов нужно принять радиус атомного ядра равным примерно 10-15 м.
Резерфорд предположил, что атом устроен подобно планетарной системе. Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца). Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
Планетарная модель строения атома по Резерфорду не смогла объяснить ряд известных фактов: электрон, имеющий заряд> должен за счет кулоновских сил притяжения упасть на ядро, а атом — это устойчивая система; при движении по круговой орбите, приближаясь к ядру, электрон в атоме должен излучать электромагнитные волны всевозможных частот, т. е. излучаемый свет должен иметь непрерывный спектр, на практике же получается иное: электроны атомов излучают свет, имеющий линейчатый спектр. Разрешить противоречия планетарной ядерной модели строения атома первым попытался датский физик Нильс Бор.
В основу своей теории Бор положил два постулата. Первый постулат: атомная система может находиться только в особых стационарных или квантовых состояниях, каждому из которых соответствует своя энергия; в стационарном состоянии атом не излучает.
Это означает, что электрон (например, в атоме водорода) может находиться на нескольких вполне определенных орбитах. Каждой орбите электрона соответствует вполне определенная энергия.
Второй постулат: при переходе из одного стационарного состояния в другое испускается или погл-щается квант электромагнитного излучения. Энергия фотона равна разности энергий атома в двух состояниях: 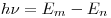 ; ; 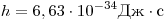 , где , где 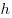 — постоянная Планка. — постоянная Планка.
При переходе электрона с ближней орбиты на более удаленную атомная система поглощает квант энергии. При переходе с более удаленной орбиты электрона на ближнюю орбиту по отношению к ядру и томная система излучает квант энергии. Теория Бора позволила объяснить существование линейчатых спектров.
 Оставить комментарий Оставить комментарий
 Сообщить об ошибке Сообщить об ошибке
| 
