|
8. Уравнение состояния идеального газа (уравнение Менделеева—Клапейрона). Изопроцессы
1. Уравнение состояния. 2. Уравнение Менделеева— Клапейрона. 3. Процессы в газах. 4. Изопроцессы. 5. Графики изопроцессов. 6. Распространенные ошибки.
Состояние данной массы газа полностью определено, если известны его давление, температура и объем. Эти неличины называют параметрами состояния газа. Уравнение, связывающее параметры состояния, называют уравнением состояния.
Для произвольной массы газа состояние газа описывается уравнением Менделеева—Клапейрона:
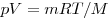 ,
где ,
где 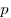 — давление, — давление, 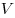 — объем, — объем, 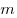 — массa, — массa, 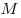 - молярная масса, - молярная масса, 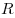 — универсальная газовая постоянная ( — универсальная газовая постоянная (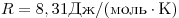 ). Физический смысл универсальной газовой постоянной в том, что она показывает, какую работу совершает один моль идеального газа при изобарном расширении при нагревании на 1 К. ). Физический смысл универсальной газовой постоянной в том, что она показывает, какую работу совершает один моль идеального газа при изобарном расширении при нагревании на 1 К.
Уравнение Менделеева—Клапейрона показывает, что возможно одновременное изменение трех параметров, характеризующих состояние идеального газа. Однако многие процессы в газах, происходящие в природе и осуществляемые в технике, можно рассматривать приближенно как процессы, в которых изменяются лишь два параметра. Особую роль в физике и технике играют три процесса: изотермический, изохорный и изобарный.
Изопроцессом называют процесс, происходящий с данной массой газа при одном постоянном параметре — температуре, давлении или объеме. Из уравнения состояния как частные случаи получаются законы для изопроцессов.
Изотермическим называют процесс, протекаю-щий при постоянной температуре: 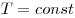 . Он описывается законом Бойля—Мариотта: . Он описывается законом Бойля—Мариотта: 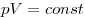 . .
Изохорным называют процесс, протекающий при постоянном объеме: 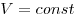 . Для него справедлив закон Шарля: . Для него справедлив закон Шарля: 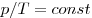 . .
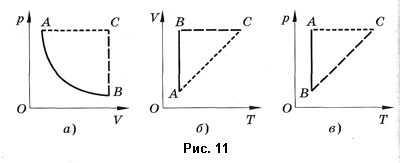
Изобарным называют процесс, протекающий при постоянном давлении. Уравнение этого процесса имеет вид 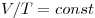 при при 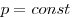 и называется законом Гей-Люссака. Все изопроцессы можно изобразить графически. На рисунке 11 представлены в различных координатах графики процессов: изотермического (изотерма АВ), изобарного (изобара АС) и изохорного (изохора ВС). и называется законом Гей-Люссака. Все изопроцессы можно изобразить графически. На рисунке 11 представлены в различных координатах графики процессов: изотермического (изотерма АВ), изобарного (изобара АС) и изохорного (изохора ВС).
Реальные газы удовлетворяют уравнению состоя ния идеального газа при не слишком высоких давлениях (пока собственный объем молекул пренебрежимо мал по сравнению с объемом сосуда, в котором находится газ) и при не слишком низких температуpax (пока потенциальной энергией межмолекулярного взаимодействия можно пренебречь по сравнению с кинетической энергией теплового движения молекул), т. е. для реального газа это уравнение и его следствия являются хорошим приближением.
 Оставить комментарий Оставить комментарий
 Сообщить об ошибке Сообщить об ошибке
| 
